Nya syntetiska metoder härledda från solvotermiska metoder, såsom jonotermiska processer, har använts för att erhålla nanopulver av LiMPO4 (M= Mn, Co och Ni), LixMSiO4 [Nytén, A. et al. (2005)] och Li- och Na-fluorofosfatbatterimaterial [DiSalvo, FJ et al.
(1971); Ellis, BL et al. (2007b)] med låg uppvärmningstemperatur. Jonotermisk syntes har uppstått när en stor mängd forskningsarbete inriktas på nya lågkostnadsprocesser för att tillverka mycket elektrokemiskt optimerade elektrodmaterial. Denna alternativa väg betraktas som en ny lågkostnadssyntesprocess eftersom den kräver mycket mindre energi än högtemperaturkeramiska vägar. Trots den högre kostnaden för joniska vätskor jämfört med vatten har det bevisats att dessa lösningsmedel kan återanvändas utan rening när de används för att framställa samma material, vilket leder till en betydande kostnadsminskning och minimerar avfallsproduktionen [Tarascon, JM. et al. (2010)]. Jonotermisk syntes har också genomförts framgångsrikt genom att använda mikrovågsugn snarare än traditionell uppvärmning, vilket minskar reaktionstiden och den energi som krävs för syntesen.
Jonotermisk syntes är baserad på användningen av en jonisk vätska som reagerande medium istället för vatten under solvotermiska förhållanden. Joniska vätskor är en klass av organiska lösningsmedel med hög polaritet och en förorganiserad lösningsmedelsstruktur [Del Popolo, MG och Voth, GA (2004)]. Rumstemperatur (eller nära rumstemperatur) joniska vätskor definieras klassiskt som vätskor vid rumstemperatur (eller <100 °C) som är gjorda av organiska katjoner och anjoner.
De har utmärkta solvatiseringsegenskaper, litet mätbart ångtryck och hög termisk stabilitet. Solvatiseringsegenskaper och fusionstemperaturer kommer att bero på kombinationen av katjoner och anjoner som väljs. Inom materialvetenskapen har det förekommit flera rapporter om joniska vätskor som används som lösningsmedel med mycket små eller kontrollerade mängder vatten involverat i syntesen [Antonietti, M et al. (2004)]. De flesta av dessa studier koncentrerade sig på amorfa material och nanomaterial.
Liksom vatten har joniska vätskor som härrör från kompatibla katjoniska/anjoniska par utmärkta lösningsmedelsegenskaper. Dessutom har de hög termisk stabilitet och försumbar flyktighet, så användningen av autoklav är inte obligatorisk. På grund av den flexibla naturen hos de katjoniska/anjoniska paren uppvisar de dessutom, som lösningsmedel, stora möjligheter att avsiktligt styra kärnbildning. Under det senaste decenniet har jonotermisk syntes utvecklats till en fördelaktig syntesteknik för framställning av zeotyper [Lin, ZJ. et al. (2008)] och andra porösa material som metallorganiska ramverksföreningar (MOF), men det har varit mycket begränsad användning av denna teknik vid syntes av oorganiska föreningar.
Det unika med jonotermisk syntes är att den joniska vätskan fungerar som både lösningsmedel och mallförsörjare. Många joniska flytande katjoner är kemiskt mycket lika arter som redan är kända som bra mallar (alkylimidazoliumbaserade, pyridiniumbaserade joniska vätskor). Många är relativt polära lösningsmedel, vilket gör dem lämpliga för upplösning av de oorganiska komponenterna som krävs för syntesen. En av de definierande egenskaperna hos joniska vätskor är deras avsaknad av ett detekterbart ångtryck, vilket effektivt resulterar i eliminering av säkerhetsproblem som är förknippade med höga hydrotermiska tryck och har också lett till deras användning i mikrovågssyntes.
I processen för jonotermisk väg, eftersom det inte finns några andra lösningsmedel tillsatta till reaktionsblandningen, hävdar teorin att inga andra molekyler finns närvarande för att fungera som rymdfyllmedel under syntesen. Detta innebär att den jonotermiska metoden idealiskt tar bort konkurrensen mellan mall–ramverk och lösningsmedel–raminteraktioner som finns i hydrotermiska preparat. Detta är emellertid det idealistiska scenariot, som inte alltid kan uppnås på grund av den möjliga nedbrytningen av en liten del av de joniska flytande katjonerna, vilket resulterar i mindre schablonkatjoner som företrädesvis kan fungera som det strukturstyrande medlet i det joniska flytande lösningsmedlet [Parnham ER och Morris, RE (2006)].
Nya molekylära modelleringsstudier indikerar att strukturerna hos joniska vätskor kännetecknas av långdistanskorrelationer och fördelningar som återspeglar katjonernas asymmetriska strukturer. Långdistansasymmetriska effekter av detta slag ökar potentiellt sannolikheten för att överföra kemisk information från mallkatjonen till ramverket, en situation som är önskvärd om full kontroll över mallprocessen ska uppnås [Parnham, ER och Morris, RE (2007) )].
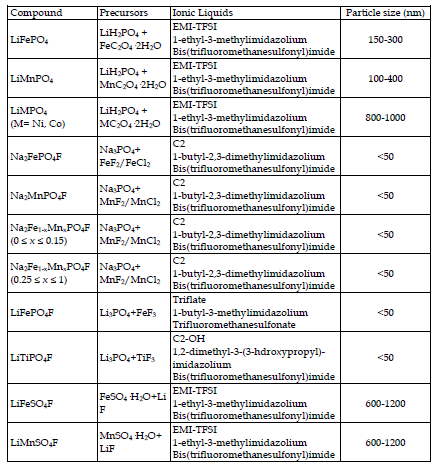
Tarascon et al. var de första att tillämpa jonotermisk syntes på batterielektrodmaterial. De testade flera joniska vätskor baserade på olika katjoniska och anjoniska arter som reagerande medium för framställning av LiFePO4-fas [Recham, N. et al. (2009a)]. De joniska vätskorna som användes visade sig ha en inverkan på LiFePO4-kärnbildning/tillväxt och att de uppförde sig som ett strukturellt styrande medel. Till exempel producerade användningen av en CN-funktionaliserad EMI-TFSI jonisk vätska [1-etyl-3-metylimidazolium-bis(trifluormetansulfonyl)imid] nålliknande pulver i [010] riktning som perfekt staplade upp för att bilda en större nål. Denna förändring på slutgruppen modifierade det reagerande mediets polära karaktär och dess solvatiseringsegenskaper och påverkade således kristalltillväxt. Blodplättsliknande partiklar längs [020] riktning skapades genom att minska polariteten genom användning av en C18-baserad EMI-katjon. Bildandet av dessa
två morfologiska slag kan förklaras i termer av konkurrerande energiytor, och det är direkt kopplat till den joniska vätskans natur, solvatiseringsförmåga, polaritet och förmåga att specifikt absorbera på en av ytorna. Beroende på de joniska vätskeegenskaperna kommer ytenergiminimering av systemet att ske via en annan mekanism. Alla LiFePO4-producerade material var elektrokemiskt aktiva, men de med bäst prestanda var av 300 och 500 nm storlekar, vilket visade 150 mAh·g-1 specifik kapacitet vid C/10 utan kolbeläggning.
Den jonotermiska processen utvidgades till syntesen av storlekskontrollerade Na-baserade fluorfosfater [Na2MPO4F (M= Fe, Mn)] [Recham, N. et al. (2009b)]. Dessa faser är attraktiva elektrodmaterial eftersom de är baserade på ekonomiska metaller och kan användas i både Li- och Na-baserade batterier. Dessutom har fluoriderna högre elektronegativitet vilket ökar joniciteten hos bindningarna och därmed deras redoxpotentialer på grund av induktiv effekt. Prover i nanostorlek av Na2FePO4F och Na2MnPO4F med en diameter på cirka 25 nm framställdes i en jonisk vätska av 1,2-dimetyl-3-butylimidazolium-bis(trifluormetansulfonylimid), i motsats till grova pulver erhållna med keramisk metod. Den elektrokemiska prestandan för järnföreningen nådde bättre resultat än den för keramiskt material, med 115 mAh·g-1, bättre initial kapacitet, lägre irreversibel kapacitet, lägre polarisation och bättre kapacitetsbevarande. Manganfasen visade inte elektrokemisk aktivitet, vilket följer den allmänna tendensen hos Mn-baserade föreningar med sämre elektrokemisk prestanda än deras Fe-motsvarighet, till exempel i LiMPO4- och Li2MSiO4-familjer. Det finns två faktorer relaterade till detta fenomen. För det första den starka Jahn-Teller-förvrängningen på Mn3+, som påverkar dess koordinationssfär; och, för det andra, den dåliga elektronisk-joniska konduktiviteten hos materialen, på grund av den större joniciteten hos MO-bindningen.
Jonotermisk process har framgångsrikt använts för att framställa nya elektroaktiva material som inte hade uppnåtts tidigare, såsom LiFeSO4F. Detta material har en adekvat struktur för att gynna Li-joners migration längs kanaler. Denna elektroaktiva fas hade inte syntetiserats tidigare eftersom den inte är tillgänglig, varken genom keramisk process eller i vattenmedium. Den sönderdelas vid temperaturer över 375ºC och i vattenmedium. Detta nya katodmaterial visade elektrokemisk aktivitet vid 3,6 V och en reversibel specifik kapacitet på 140 mAh·g-1, mycket nära den teoretiska specifika kapacitetsvärdet på 151 mAh·g-1. Således har denna förberedande process visat sig vara ett användbart verktyg för att syntetisera nya och kända elektroaktiva material i nanostorlek.
